Glokomda Beyin Hasarı: Glokom Gerçekte Tüm Görme Yollarının Dejeneratif Bir Hastalığı mıdır?
Dr. Kaya N. Engin
Sağlık Bilimleri Üniversitesi, Ümraniye Eğitim ve Araştırma Hastenesi
Glokom progresif optik sinir hasarı ve görme kaybı ile karakterize bir oküler hastalıklar gurubudur. Geri dönüşümsüz körlüğün en sık nedeni olarak bilinen glokom, progresif retinal ganglion hücre kaybı ile karakterize olmasına karşın yıllarca “göziçi basınç (GİB) artışına bağlı bir hastalık” olarak algılanagelmiştir. Günümüzde ise artmış GİBının glokom tanımından çıkarılarak majör risk faktörü olarak kabul edilmesine ve glokomun bir optik nöropati olarak tarif edilmesine karşın, klinik uygulamalar halen ağırlıklı olarak GİBını düşürmeye yöneliktir. Bugün GİBını düşürmeye yönelik elimizde etkin tıbbi ve cerrahi tedaviler olmasına rağmen progresif görme kaybı glokom olgularında yaygın görülmeyi sürdürmektedir (1). Üretilen nöroprotektif stratejiler gerek reseptör ve iyon kanallarının çeşitliliği, gerekse yan etkilerinin ağırlığı nedeni ile sınırlı kullanıma sahiptirler. Ayrıca klinik çalışmalar henüz yeterli değildir (2). Glokomda retina gangliyon hücre korunmasının önemi bazı araştırmacıları daha ileri bazı açılımlara itmiş, optik nöropatinin optik sinir ve trakt yolu ile bir santral sinir sistemi patolojisi olarak değerlendirilebileceği fikrini doğurmuştur.
Glokom takibinde en yaygın kullandığımız yöntem santral görme alanı (SGA)dır. Aslında SGAdaki bir defekt retinadan kortekse herhangi bir yere ait bir patolojiye bağlı olarak gelişebilir (3). Geleneksel olarak gözardı edilen bu gerçek, ve glokom-beyin ilişkisi üzerine son yıllarda yoğunlaşan çalışmalar, GİBndan bağımsız tedavi stratejilerinin geliştirilmesinde retina ve optik sinir başının gerisinin de göz önüne tutulması, dahası glokom tanı ve takibinde beyindeki nörodejeneratif yayılımın dikkate alınması gerektiğini bizlere göstermiştir (4). Nitekim normotensif glokomda beyin MRında iskemi gözlenen hastalarda SGAda daha derin depresyonlar gözlendiği bildirilmiştir (5). Glokom hastalarında görülen nöron popülasyonlarında selektif kayıp, hasarlı nöron ile sağlam komşu nöron arasında transsinaptik dejenerasyon, hücre hasar ve ölümünde ortak mekanizmalar, Alzheimer, Parkinson gibi nörodejeneratif hastalıklarda gözlenenler ile benzerlikler de göstermektedir (6).
Anatomik yapıyı kabaca anımsarsak, santral görme yolları retina, optik sinirler, optik kiezma, optik traktlar, korpus genikulatum laterale (CGL) –lateral genikulat nukleus (LGN)u kapsar, diğer beyin sapı pirimer görsel nukleuslar, hipotalamik nukleus, optik radyasyon, görsel korteks olarak sıralayabiliriz. Bu yapıda optik kiezmanın bizim açımızdan önemi ise, her iki globdan gelen optik sinirlerin temporal lifleri direk geçerken nasal liflerin çapraz yaparak karşı trakta geçmelerinden kaynaklanır. Pirimer görsel korteks striate korteks, alan 17, deneysel çalışmalarda sıkça kullanılan V1 adları ile anılmaktadır (7).
Gupta N ve Yücel YH 2003 yılında farelerde oluşturdukları tek taraflı deneysel glokom modellerinde, lateral genikulat nukleuslarda GİB ve optik sinir başı hasarı ile orantılı magno-, parvo-, konioselüler yolaklarda retinal ganglion hücre hasarı, ayrıca yine bu hasar ile orantılı vizüel korteks incelmesini bildirmişlerdir (6). Ayrıca, benzer lezyonlar maymunlarda da gösterilmiş, nöroprotektif droglar arasında adı geçen Memantin ile lateral genikulat nukleuslardaki nöron hasarının önlenebildiği bildirilmiştir (8). İnsanlarda retrobulber görme yollarında hasar ise ilk kez Gupta N ve ark. tarafından 2006 yılında gösterilmiştir (9). Bu çalışmada 79 yaşında glokomlu bir hastanın ölümü sonrası otopside alınan dokuları eski klinik bulguları ile birlikte değerlendirilmiş, ayrıca aynı yaş gurubundan 4 hastanın otopsi preperatları ile karşılaştırılmıştır. Glokomlu hastada optik sinir sajital kesitte inferior akson kaybı ve atrofiye bağlı küçülme, lateral genikulat nukleuslarda magnoselular ve parvoselular nöronlarda küçülme ve dejenerasyon, görsel kortekste ise belirgin incelme bildirilmiştir (Resim 1).
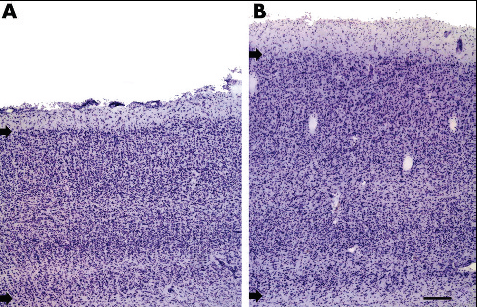
Resim 1: Görsel korteksde glokom hastasında (A) gözlenen incelme aynı yaştaki sağlıklı bireyle (B) karşılaştırıldığında daha net gözlenmektedir (Gupta ve ark., 2006).
Bu çalışmaların ışığında glokom tedavisinde GİB bağımsız stratejilerin önemi artarken, glokom hastalarında beyin hasarını in vivo gösterme çabaları hız kazanmıştır. Bu amaçla en çok yararlanılan teknoloji ise manyetik rezonans (MR) görüntülemedir. Optik sinir çapı bireyler arasında 4-9 mm gibi önemli bir farklılık gösterebilir (10), ancak bu anatomik yapı glokomatöz beyin hasarını görüntülemede en önemli odak noktası olmuştur. Glokom hastalarında konvensiyonel MR ile yapılan bir çalışmada, optik sinir çapının kontrole göre anlamlı küçük, optik kiazmanın kısa olduğunu ve bu bulguların c/d oranlarından çok MD değerlerinde bozulma ile korelasyon gösterdiği bildirilmiştir (11). Bu alan için en geniş vaka serili çalışmalardan birinde ise (47 kişi), 3T ultrafast high-resolution MR kullanılmış ve optic sinir çapının retina sinir lifi kalınlığı ile korele olduğu gösterilmiştir (12). Pirimer açık açılı glokomlu, 26 hasta ve 26 kontrol üzerinde rutin MR teknikleri ile yapılan çalışmada glokomun optik sinir atrofisi ve dejenerasyonuna neden olduğu bildirilmiş, ayrıca aynı çalışmada ortaya çıkarılan artmış ak madde hiperintensitesi bulgusu da pirimer açık açılı glokom patogenezinde serebrovasküler iskeminin rolü olabileceği yönünde değerlendirilmiştir (13).
CGLlerin görüntülenmesi ve analizi ise büyük bir sorun teşkil etmektedir zira bu yapı glokomatöz hasarın belirgin olduğu bölgelerdendir (6,8,9). Fonksiyonel serebral kan akım değişimlerini direk ölçen Arterial Spin Labeling fMRI yöntemi Lu ve arkadaşları tarafından 5 sağlıklı bireyde başarıyla kullanılmıştır (14). Ancak CGLnin DTI ile yapısal olarak incelenmesi yapısında intact ak madde bulunmaması nedeni ile tartışmalıdır. CGL, optic trakt lifleri ile çevrelenmiş, retina ile görsel korteks arasında bir işlem istasyonu olarak görev alan kompleks bir yapıdır. Toplam 6 laminadan oluşur, bunların 3ü çaprazlanma gösteren, 3ü ise çaprazlanma göstermeyen liflerden oluşur. En dipteki 2 lamina (1 çaprazlanma gösteren, 1 göstermeyen) magnoselülerdir ve hareket algısından sorumlu retinal “M” gangliyon hücrelerinden akson alır. Diğer 4 parvoselüler lamina ise renk ve ayrıntı algısından sorumlu “P” hücrelerinden akson almaktadır (15). Optik trakt insanlarda CGLden görsel korteksdeki Kalkarin Sulkusa kadar DTI ile görüntülenebilmiştir. Bu çalışmada CGLlerden ROI alınmış ancak herhangi bir analiz yapılmamıştır (16). Ancak Talamus ve basal gangliyonlar gibi kompleks ak ve gri madde içeren nöral yapıların DTI ile gösterilebileceği ve akım analizlerinin yapılabileceği literatürde mevcuttur (17). Bir diğer DTI çalışmasında, migrenli hastalarda sol LGNda düşük FA değerleri bildirilmiştir (18). Bizim bilgimiz dahilinde, literatürde glokomatöz CGL hasarını bildiren bir klinik çalışma mevcut değildir. Bizim bir çalışmamızda ise (19), glokom hastalarında CGL DTI analizleri ile göz bulguları arasında istatistiksel açıdan anlamlı korelasyon gösterilmiş, ancak bu korelasyon negatif bulunmuştur. Kompleks nöral yapılarda diffüzyon anisotropisi, miyelinizasyon derecesi, çapların dağılımı, ak ve gri madde arasında diffüzyon dağılımı ve aksonların düzen koherensi gibi pekçok faktörden etkilenmektedir (18). Her ne kadar CGL bulgularımız kendi içinde uyumlu iseler de, henüz bilinmeyen bu alanda bulgularımızın gerek ileri DTI çalışmaları ile aydınlatılmaları, gerekse geniş vaka serileri ile doğrulanmaları gerekmektedir.
Optik radyasyon ipsilateral gözle ilgili bilgi vermese de, ROI alımı kolaylığı nedeniyle sıkça çalışılmıştır. 50 glokom 50 sağlıklı bireyden oluşan bir çalışmada ipsilateral gözün etkilendiği bildirilmiş ve bu durum mikroanjiyopatik lezyonlarla açıklanmıştır (20). Yeni bir makalede ise optic radyasyon DTI analizinin açık açılı glokom için %94.1, normotensive glokom için ise %100 doğrulukta glokom tesbitinde kullanılabileceği bildirilmiştir (21).
Anatomik olarak değerlendirildiğinde, glokomatöz hasarın gösterildiği yapılar arasında en uzak olan ise görme yollarının sonlandığı oksipital korteksdir (7). Ancak bu yapı ile ilgili de glokom özelinde çok değerli çalışmalar gerçekleştirilmiştir. İyi uyaran alamayan korteks alanında düşük N-Asetilaspartat düzeyini tesbit eden Oksipital Proton MR Spektroskopi tekniği ile kronik glokomlu farelerde görsel korteksde kolin ve glutamat düzeylerinde azalmayı, kreatin düzeyinde ise artmayı ortaya çıkarmıştır (22). Bu teknik insanlarda da glokom ve yaşa bağlı makula dejeneransı olan hastalarda denenmiştir. Ancak yukarıdaki hayvan deneyinin tersine, bu hastalarda ilerleyici görme alan defekti ile uyumlu alanlarda metabolit düzeylerinde bir azalma gözlenmemiştir (23).
Bu alanda en önemli bulgular fMRI ile elde edilmiştir. fMRI, uyarı alan korteks alanında kan oksijen düzeyinin artması ve kan oksijen düzeyi bağımlı (BOLD) MR sinyallerinin oluşması prensibine dayanır. BOLD sinyalleri haritalamakta ise Retinotopik Organizasyon kullanılır. Duncan ark. glokom hastalarında görme alan defektlerine uyan görsel korteks alanlarında BOLD sinyal azalmasını tesbit ederek, glokom beyin ilişkisini insanlarda in vivo göstermişlerdir (24).
MR ile görme yollarını görüntülemede kullanılabilecek bir diğer yöntem DTIdir. Sıvıların sinir trasesi boyunca bir düzlem içinde hareket prensibine dayalı bu yöntem ile 3 yöne sıvı difüzyonunun tam tanımı yapılabilir. Radyal (λ1) ve aksiel diffüziviteler (λ2, λ3) elde edilerek fraksiyonel anisotropi (FA)ler hesaplanabilir. Sıvı anisotropi haritaları çıkarılarak bir sinir trasesi boyunca görüntülenebilir ve bu işleme “Traktografi” adı verilir (25) İnsanlarda bu yöntem ile optik traktın, Korpus Genikulatum Laterale (CGL)den kalkarin sulkusa kadar görüntülenmesi başarılmıştır (16).
Glokom beyin ilişkisini, -klinik kullanımda olan- 1,5 Tesla MR cihazı ile kliniğimizde de inceledik. Bu çalışmalarımız 2006 ile 2014 yılları arasında devam etti. Bu şekilde glokomda göz beyin bağlantısını insanda noninvazif ve kapsamlı olarak göstermeyi hedefledik. Bu ön çalışmalarımızın bizim açımızdan önemli bir amacı da, gelecekte geniş vaka serileri yada klinik taramalar yapılabilmesi için kliniklerde rutin kullanılabilen MR cihazlarına uygun görüntüleme ve analiz teknikleri geliştirebilmek idi. Bu alandaki öncü klinik çalışmalar ve hayvan deneyleri genelde deneysel amaçlı kullanılan 3 veya tamamen deneysel kullanılan 6-7 Tesla MR cihazlarında gerçekleştirilmiştir. Ayrıca literatürde, yapısal ve fonksiyonel klinik göz tanı yöntemleri ile DTI ve fMRI tekniklerini birlikte irdeleyen bir çalışma bulunmamaktadır.
Bir pilot çalışma niteliğinde olan ilk yayınlarımızda öncelikli olarak DTI ile yapısal olarak ve fMRI ile fonksiyonel olarak glokomatöz beyin hasarını değerlendirebilecek ve görüntüleyecek yöntemler oluşturmaya gayret ettik (26). MedINRIA programı kullanılarak difüzyon tensor haritaları ve fiber traktoları oluşturuldu. Yıllar içerisinde görüntüleme anlamında ilerleme kaydedebildik (Resim 2). Ayrıca aynı bölgeden alınan b0 koronal plan görüntülerde büyütme uygulanarak, optik sinir morfolojileri bu planda da değerlendirildi (Resim 3).
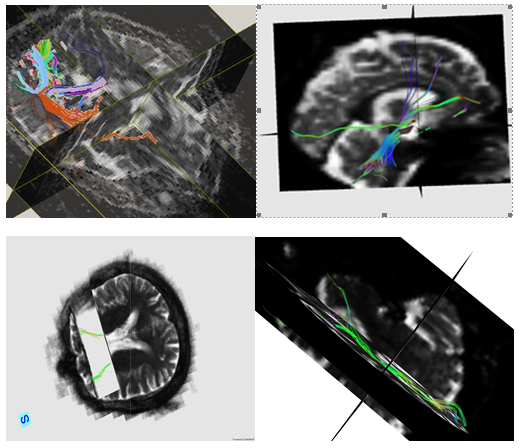
Resim 2: Optik sinirlerin “Traktografi” metodu ile görüntülenmesinde 2009-2011 yılları arasında çlışma rubu olarak kaydettiğimiz ilerlemeler.
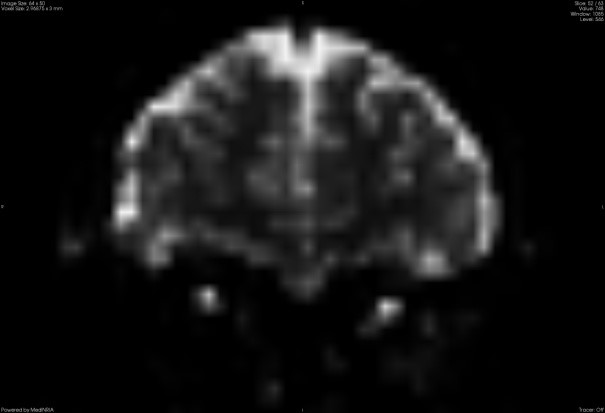
Resim 3: Bir hastamızda b0 koronal plan görüntülerde optik sinirlerin DTI kullanılarak görüntülenmesi.
Ayrıca geliştirdiğimiz özgün teknikler kullanılarak optik sinir (Resim 4) ve CGL bölgesinde ilgi bölgeleri (ROI) işaretlendi.Sonrasında, seçilen bölgerde DTI parametre ölçümleri yapıldı.

Resim 4: DTI ile diffüzyon analizi için optic sinirlerden ROI alımı.
fMRI çekimleri de 1.5 T MR cihazıyla yapıldı. Glokomlu hastalardan sağ ve sol göz için ardarda iki ayrı çekim yapıldı. Görsel kortekste meydana gelen aktivasyonları karşılaştırabilmek için her hastada glokomun en çok etkilediği görsel alan bölgeleri belirlendi ve bu bölgelerin uyarılması sırasında oluşan aktivasyonlar hesaplandı. Bunun için her bölgenin SPM(t) haritalarında eşik değerini geçen voksel kümeleri bulundu ve bunların fMRI karşılıkları kullanılarak yüzde BOLD değişim miktarı ölçüldü (Resim 5).

Resim 5: Belirli voksellerde BOLD sinyalinin tesbit edilmesi
Bu teknikleri kullanarak yaptığımız ilk klinik çalışmada ise DTI verilerini göz bulguları ile karşılaştırarak göz ve göz arkası lezyonların devamlılığını dar bir vaka serisinde gösterebildik (19).Glokomda optik sinir dejenerasyonu ise in vivo ilk kez Hui ve ark. tarafından, 28 gün boyunca deneysel glokom indüksiyonu yapılan farelerde DTI ile gösterilmiştir (27). insanda da DTI ile glokom hasarı Garaci ve ark. Tarafından 3T MR ile incelenmiş, özellikle FA değerlerinde glokomlu hastalarda anlamlı düşme gözlenmiştir (28). Yine insanda, bu kez ORler 3T MR ile 50şer glokom hastası ve kontrolde incelenmiş, ve ORlarda retrograd transnöronal rarefaksiyonlar bildirilmiştir (29).
fMRI analizlerinde ise hassas alan analizinde, tüm voksellerde BOLD alınamadığından başarılı olunamadı. Ancak asimetrik tutulumlu hastalarda daha ağır defektli gözdeki BOLD değerleri diğer göze göre düşük bulundu (19). Duncan ve ark. ın (24) önemli çalışması halen literatürde SGA ve fMRI ile glokomda fonksiyonel analiz yapılmış tek çalışmadır. Bu çalışmada uzun ve komplike bir uyaran kullanılarak 3T MR ile, SGAdaki bir defektin korteksde görüntülenmesi başarılmıştır. Bu hassas analizlerin bizim kullandığımız mültifokal haritalama yöntemi ile de yapılması mümkündür ancak, bu yöntemin orjinalinde de 3T MR kullanılmıştır (30).
Çalışma grubumuzun henüz yayınlanmamış, 65 glokom hastasının 130 gözünün dahil edildiği çalışma ise halen literatürdeki en geniş glokom olgu serisine sahip DTI çalışmasıdır (31). Bu çalışmada OCT ve SGA bulguları kaydedildi. Optik sinir ve distal görme yollarını teşkil eden optik radyasyon görüntüleri 1,5T diffüzyon-tensor MR ile 3D-T1 ağırlıklı görüntülendi. Geliştirdiğimiz yöntemlerle alınan kesit ve çizilen traktografilerde sinir dokularının diffüzyon parametreleri (FA, ADC, λ) hesaplandı. Hastalar arasında bir karşılaştırma yapılmayarak, göz ve görme yolları verilerinin korelasyonları istatistiksel olarak değerlendirildi. Optik sinir deformasyonu hem B0 coronal plan hem traktografilerde gösterildi. Diffüzyon analizlerde ise, özellikle gangliyon hücre sayısının optik sinir difizyon parametreleri ile yüksek korelasyon gösterdiği tesbit edildi. Korelasyon özellikle λ1 ve l┴ parametrelerinde çok yüksek bulundu. Geniş olgu serili bu çalışmamız da, glokomatöz nörodejenerasyonun göz ve görme yollarındaki bütünlüğünü ortaya koymuştur.
Daha ileri çalışmalarda ise optik sinir çapı (32) ve hacminin (33) 3T MR ile ölçülmesinin glokomatöz optik atrofideki akson kaybının klinik işareti olarak kabul edilebileceği bildirilmiştir. Chang ve ark. (34) 27 hastada c/d oranı ve glokom evresinin, Sidek ve ark. (35) ise 60 hastada retina sinir lifi kalınlığı ve glokom evresinin optik sinir DTI parametreleri ile uyumlu olduğunu bildirmişlerdir. Son olarak Li ve ark. (36)ın mevcut glokom DTI çalışmalarından yaptıkları meta-analize göre, optik sinir ve radyasyonda diffüzyon parametrelerinden FA nın anlamlı azalması ve MDnin anlamlı yükselmesi glokom hasarının ağırlığının göstergesi kabul edilebilir.
SON SÖZ:
YH Yücel ve N Gupta, glokom-beyin bağlantısı üzerine yıllarca süregelen çalışmalarının sonrasında şu ifadeyi kullanmışlardır: “Glokomun nörodejeneratif bir hastalık olduğu, görme sistemindeki nöral hasarı anlama yolunda işlevsel bir hipotezdir. Bugünkü bilgilerin bize anlattığı, göz içi basıncından bağımsız mekanizmaların glokomatöz dejenerasyonda etkili olduğudur. Bu paradigma, glokom hastalarında görme kaybını önleyecek yeni, göz içi basıncından bağımsız stratejilerin keşfi yolunu açabilir.”
Göz içi basıncından bağımsız, optik sinir başının ötesini de kapsayan stratejiler glokomun değerlendirilmesi ve tedavisi açısından gereklidir. Bugün için görme yollarını optik sinir başından görsel kortekse kadar görüntülemek mümkündür. Bu bağlantıyı daha net açığa çıkarabilecek sofistike yöntemler de halen geliştirilmektedir. Ancak bizim çalışmamızın gösterdiği üzere, rutin klinik aygıtlar glokom-beyin bağlantısını göstermek ve incelemek için yeterlidir.
Bir optik nöropati olan glokomun, göz ve tüm santral görme yollarının nörodejeneratif bir hastalığı olduğunu destekleyen veriler artmaktadır. Retrobulber glokomatöz hasarın daha iyi anlaşılması glokom tanı, takip ve tedavisinde daha etkili stratejiler geliştirmemizi kolaylaştıracak ve bu gizemli hastalıkla ilgili halen yanıtlayamadığımız sorulara yaklaşımımızı zenginleştirecektir.
KAYNAKLAR
- Chidlow G, Wood JP, Casson RJ. (2007). Pharmacological neuroprotection for glaucoma. Drugs 67(5): 725-759.
- Weinreb RN. (2007). Glaucoma neuroprotection: What is it? Why is it needed? Can J Ophthalmol. 42(3): 396-398.
- Landers J, Tang KC, Hing S. (2004). A visual field abnormality: ocular or cerebral cause? Clin Experiment Ophthalmol. 32(2): 219-222.
- Yücel YH, Zhang Q, Weinreb RN, Kaufman PL, Gupta N. (2003). Effects of retinal ganglion cell loss on magno-, parvo-, koniocellular pathways in the LGN and visual cortex in glaucoma. Prog Retin Eye Res. 22(4): 465-481.
- Suzuki J, Tomidokoro A, Araie M, Tomita G, Yamagami J, Okubo T, Masumoto T. (2004). Visual field damage in normal-tension glaucoma patients with or without ischemic changes in cerebral magnetic resonance imaging. Jpn J Ophthalmol 48(4): 340-344.
- Gupta N, Yücel YH. (2003). Brain changes in glaucoma. Eur J Ophthalmol 13(Suppl 3): S32-535.
- Sadun AA, Glaser JS, Bose S. (2007). Anatomy of the Visual Sensory System, In: Duane's Ophthalmology, Tasman W, Jaeger EA, (Eds.), Chapter 34, Lippincott Williams & Wilkins, ISBN 978-0-7817-6855-9, Philadelphia, PA, USA.
- Gupta N, Yücel YH. (2007). Glaucoma as a neurodegenerative disease. Curr Opin Ophthalmol 18(2):110-114.
- Gupta N, Ang LC, de Tilly LN, Bidaisee L, Yucel YH. (2006). Human glaucoma and neural degeneration in intracranial optic nerve, LGN, and visual cortex. Br J Ophthalmol 90: 674–678.
- Stark DD, Bradley WG. (1996). Magnetic Resonance Imaging In: Orbit, Scott W. Pp 988-1028. Mosby, Missouri,USA.
- Kashiwagi K, Okubo T, Tsukahara S. (2004). Association of magnetic resonance imaging of anterior optic pathway with glaucomatous visual field damage and optic disc cupping. J Glaucoma 13(3): 189-195.
- Lagrèze WA, Gaggl M, Weigel M, Schulte-Mönting J, Bühler A, Bach M, Munk RD, Bley TA. (2009). Retrobulbar optic nerve diameter measured by high-speed magnetic resonance imaging as a biomarker for axonal loss in glaucomatous optic atrophy. Invest Ophthalmol Vis Sci. 50(9): 4223-4228.
- Kitsos G, Zikou AK, Bagli E, Kosta P, Argyropoulou MI. (2009). Conventional MRI and magnetisation transfer imaging of the brain and optic pathway in primary open-angle glaucoma. Br J Radiol. 82(983): 896-900.
- Lu K, Perthen JE, Duncan RO, Zangwill LM, Liu TT. (2008). Noninvasive measurement of the cerebral blood flow response in human lateral geniculate nucleus with arterial spin labeling fMRI. Hum Brain Mapp. 29(10): 1207-14.
- Fitzgerald MJT, Folan-Curran J. (2002). Central Visual Pathways, In: Clinical Neuroanatomy and Related Neuroscience, Fitzgerald MJT, Folan- Curran J (Eds), Chapter 25, W.B. Saunders, ISBN 0702 025585, Spain. Pp235
- Sherbondy AJ, Dougherty RF, Napel S, Wandell BA. (2008). Identifying the human optic radiation using diffusion imaging and fiber tractography. J Vis. 8(10): 1-11.
- Mukherjee P, Miller JH, Shimony JS, Philip JV, Nehra D, Synder AZ, Conturo TE, Neil JN, McKinstry C. (2002). Diffusion-tensor MR imaging of gray and white matter development during normal human brain maturation. AJNR 23(9): 1445-1456.
- Granziera C, DaSilva AF, Snyder J, Tuch DS, Hadjikhani N. (2006). Anatomical alterations of the visual motion processing network in migraine with and without aura. PLoS Med. 3(10): e402.
- Engin KN, Yemişci B, Töreyen-Bayramoğlu S, Turan-Güner N, Özyurt O, Karahan S, Öztürk C, Çağatay P. (2014). Structural and functional evaluation of glaucomatous neurodegeneration from eye to visual pathways using 1,5T MRI: A pilot study. J Clin Exp Ophthalmol. 5(3): 1000341.
- Murai H, Suzuki Y, Kiyosawa M, Tokumaru AM, Ishii K, Mochizuki M. (2013). Positive correlation between the degree of visual field defect and optic radiation damage in glaucoma patients. Jpn J Ophthalmol. 57(3): 257-262.
- El-Rafei A, Engelhorn T, Wärntges S, Dörfler A, Hornegger J, Michelson G. (2013). Glaucoma classification based on visual pathway analysis using diffusion tensor imaging. Magn Reson Imaging 31(7): 1081-1091.
- Chan KC, So KF, Wu EX. (2009). Proton magnetic resonance spectroscopy revealed choline reduction in the visual cortex in an experimental model of chronic glaucoma. Exp Eye Res. 88(1):65-70.
- Boucard CC, Hoogduin JM, van der Grond J, Cornelissen FW. (2007). Occipital proton magnetic resonance spectroscopy (1H-MRS) reveals normal metabolite concentrations in retinal visual field defects. PLoS ONE 2(2): e222.
- Duncan RO, Sample PA, Weinreb RN, Bowd C, Zangwill LM. (2007). Retinotopic organization of primary visual cortex in glaucoma: Comparing fMRI measurements of cortical function with visual field loss. Prog Retin Eye Res. 26(1): 38-56.
- Nucifora PGP, Verma R, Lee S, Melhem ER. (2007). Diffusion-Tensor MR Imaging and Tractography: Exploring Brain Microstructure and Connectivity. Radiology 245: 367-384.
- Engin KN. (2011) Functional and structural evaluation of retrobulbar glaucomateus damage. In: Kubena T, (Eds.), The Mystery of Glaucoma, In Tech Inc, Rijeka, Croatia: p. 293-307.
- Hui ES, Fu QL, So KF, Wu EX. (2007). Diffusion tensor MR study of optic nerve degeneration in glaucoma. Conf Proc IEEE Eng Med Biol Soc. 20072007: 4312-4315.
- Garaci FG, Bolacchi F, Cerulli A, Melis M, Spanò A, Cedrone C, Floris R, Simonetti G, Nucci C. (2009). Optic nerve and optic radiation neurodegeneration in patients with glaucoma: in vivo analysis with 3-T diffusion-tensor MR imaging. Radiology 252(2): 496-501.
- Engelhorn T, Michelson G, Waerntges S, Struffert T, Haider S, Doerfler A. (2011). Diffusion Tensor Imaging Detects Rarefaction of Optic Radiation in Glaucoma Patients. Acad Radiol. 18(4): 764-769.
- Vanni S, Henriksson L, James AC. (2005). Multifocal fMRI mapping of visual cortical areas. Neuroimage 27(1): 95-105.
- Engin KN, Yiğit U, Töreyen-Bayramoğlu S, Turan-Güner N, Özyurt O, Tufan K, Ağaçhan A, Taşkapılı M, Çağatay P. (2015). Clinical Evaluation of the Eye-to-visual-pathway Integrity of Glaucomatous Neurodegeneration Using 1.5T MR Imaging. SOE Vienna, Austria.
- Ramli NM, Sidek S, Rahman FA, Peyman M, Zahari M, Rahmat K, Ramli N. (2014). Novel use of 3T MRI in assessment of optic nerve volume in glaucoma. Graefes Arch Clin Exp Ophthalmol. 252(6): 995-1000.
- Nucci C, Mancino R, Martucci A, Bolacchi F, Manetti G, Cedrone C, Culasso F, Floris R, Cerulli L, Garaci FG. (2012). 3-T Diffusion tensor imaging of the optic nerve in subjects with glaucoma: correlation with GDx-VCC, HRT-III and Stratus optical coherence tomography findings. Br J Ophthalmol. 96(7): 976-980.
- Chang ST, Xu J, Trinkaus K, Pekmezci M, Arthur SN, Song SK, Barnett EM. (2013). Optic nerve diffusion tensor ımaging parameters and their correlation with optic disc topography and disease severity in adult glaucoma patients and controls. J Glaucoma. 23(8): 513-520.
- Sidek S, Ramli N, Rahmat K, Ramli NM, Abdulrahman F, Tan LK. (2014). Glaucoma severity affects diffusion tensor imaging (DTI) parameters of the optic nerve and optic radiation. Eur J Radiol. 83(8): 1437-1441.
- Li K, Lu C, Huang Y, Yuan L, Zeng D, Wu K. (2014). Alteration of fractional anisotropy and mean diffusivity in glaucoma: novel results of a meta-analysis of diffusion tensor imaging studies. PloS One. 9(5): e97445.



